Tirpumas - tai medžiagos (dujų, skysčio ar kieto kūno), vadinamos tirpiniu, savybė ištirpti skystame tirpiklyje, sudarant vientisą tirpalą. Tirpumas stipriai priklauso nuo tirpiklio, temperatūros ir slėgio.
Dujų tirpumui išreikšti dažniausiai naudojami tūrio vienetai (ištirpusių dujų tūris, tenkantis vienam tūriui tirpiklio). Veiksniai, turintys įtakos dujų tirpumui skysčiuose, yra svarbūs gamyboje. Norint padidinti anglies dioksido kiekį gazuotame vandenyje ir šampane, jų gavimo procesas atliekamas padidintame slėgyje ir palyginti žemoje temperatūroje.
Tirpumas gali būti labai įvairus, nuo begalinio (etanolis vandenyje), iki labai menko (sidabro chloridas vandenyje). Dujų tirpumas yra tiesiogiai proporcingas tų dujų parcialiniam slėgiui virš tirpiklio. Daugelis kietų tirpinių vandenyje tirpsta geriau, kai temperatūra aukštesnė. Skystiems ir kietiems tirpiniams slėgis turi mažai įtakos.
Apskritai, poliniai junginiai geriau tirpsta poliniuose tirpikliuose (pvz., vandenyje), tuo tarpu nepoliniai - nepoliniuose. Pavyzdžiui, labai polinis (hidrofilinis) junginys šlapalas puikiai tirpsta labai poliniame vandenyje, sunkiau - mažiau poliškame metanolyje, ir praktiškai netirpsta nepoliniame benzene.
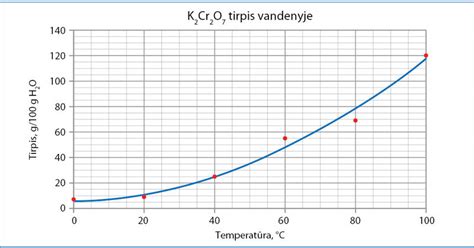
Tirpumo priklausomybė nuo temperatūros
Propano dujų tirpumas vandenyje
Propano dujos netirpsta vandenyje pagal jo cheminę prigimtį. Tai angliavandenilių dujos, turinčios ne polinius ryšius, skirtingai nei vanduo, turintis polinius ryšius. Tai sukuria ryšį tarp to paties tipo ryšių ir atotrūkio tarp skirtingų.
Propano dujos (C3H8) yra bespalvės ir bekvapės. Jo cheminė sudėtis susideda iš trijų anglies atomų grandinės, turinčios aštuonias vandenilio atomus, todėl joms būdingos paprastos ir stabilios jungtys.
Poliškumas ir jo svarba
Chemijoje molekulės poliškumas reiškia įkrovos pasiskirstymą molekulėje, ir tai priklauso nuo to, kaip atomai yra apgyvendinami ir kaip suformuojamos jų jungtys.
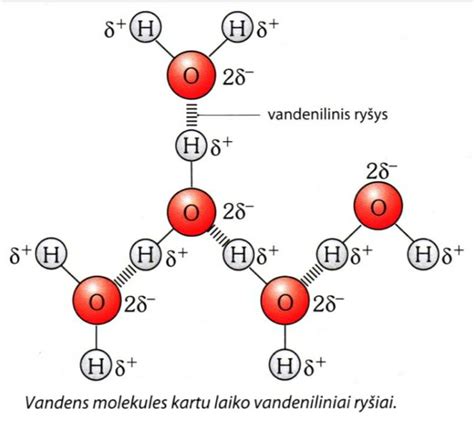
Vanduo yra polinė molekulė. Deguonies atomas, dėl kurio jis turi didesnį tūrį, palyginti su vandenilio atomais, yra neigiamas. Vandenilio atomai, kurie yra du ir mažesni, juda ta pačia kryptimi. Kadangi jie turi teigiamą krūvį, vandens molekulė vienoje pusėje išlieka neigiama, o kita - teigiama.
Kita vertus, propano dujos turi struktūrą, kurioje atomai, kurie jai suteikia savo struktūrą, yra anglis. Anglis neturi gerai apibrėžto krūvio, todėl ryšys tarp anglies yra neutralus.
Propano molekulės struktūra
Praktinė reikšmė
Praėjusiame amžiuje propanas kartu su kitais angliavandeniliais buvo labai svarbus civilizacijai. Žinant šio junginio chemines savybes, labai svarbu išgauti, valyti, apdoroti ir transportuoti, be kita ko.
Didelį propano dujų panaudojimą galima pamatyti daugelyje namų, kur jis naudojamas kaip kuras krosnims ir vandens šildymui. Transporto srityje taip pat pastebimas didelis poveikis, nes kelios agentūros nusprendė investuoti į transporto priemones, kurios dirba su propano dujomis.
Naudojant propano dujas būtina atsižvelgti į tai, kad jis yra lakus produktas, todėl jis turi būti saugioje vietoje, esant vidutinei temperatūrai ir atokiau nuo to, kas gali sukelti trumpą jungimą. Propano dujos yra bekvapės, todėl sunku aptikti nutekėjimo atveju. Kartais pridedamas priedas, kad žmogaus nosis galėtų jį atpažinti, tačiau svarbu nepamiršti, kad jis neturi kvapo. Rekomenduojama turėti dujų detektorius tokiose vietose, kur naudojamos tokios medžiagos.
Kaip paruošti įrangą dujų surinkimui vandens išstūmimo būdu
Dujų surinkimo būdai
Atsižvelgiant į dujų santykinį tankį, dujas galima surinkti į tam tikrą indą išstumiant orą:
- Sunkesnės už orą dujos orą išstumdamos leisis žemyn, tai tokias dujas surinksime leisdami į indą, kurio dugnas yra apačioje. Pavyzdžiui, mėgintuvėlį.
- Lengvesnės už orą dujos orą išstumdamos kils į viršų, tai tokias dujas surinksime leisdami į indą, kurio dugnas yra viršuje. Pavyzdžiui, apverstą mėgintuvėlį.
Dujas galima surinkti į mėgintuvėlį išstumiant iš jo vandenį. Pagrindinė sąlyga - dujos turi būti netirpios vandenyje.
Dujų surinkimas išstumiant vandenį
Tokių dujų, kaip NH3, HCl, SO2, Cl2 nerinksime vandens išstūmimo metodu, nes jos yra tirpios vandenyje. O2, H2, N2, CO2 galime rinkti išstumiant vandenį, nes jos yra netirpios (arba labai mažai tirpios) vandenyje.
Skysčiuose ištirpusios dujos pašalinamos tuos skysčius ilgai virinant. Taip gaunamas distiliuotas vanduo be anglies dioksido, naudojamas laboratorijose tikslioms analizėms atlikti. Ištirpę elektrolitai sumažina dujų tirpumą paimtame skystyje. Pagamintas dujinis chloras laikomas virš valgomosios druskos tirpalo, nes sumažėja jo nuostoliai dėl jo tirpumo vandenyje.
Temperatūros įtaka dujų tirpumui
Dujų tirpimo procesas dažniausiai yra egzoterminis, todėl (pagal Le - Šatelje principą) Pastovioje temperatūroje dujų tirpumas skysčiuose yra tiesiogiai proporcingas slėgiui, H2O). Nepolines molekules turinčios dujos geriau tirpsta nepoliniuose tirpikliuose (Ne, Ar, H2, N2 + benzenas). Su tirpikliu reaguojančios dujos dažnai pasižymi geru tirpumu (SO3 + H2O → H2SO4; 2NO2 + H2O → HNO2 + HNO3).
Fizikinės savybės: Vandenilis H2 yra bespalvės, bekvapės dujos, blogai tirpstančios vandenyje, lengvesnės už orą.