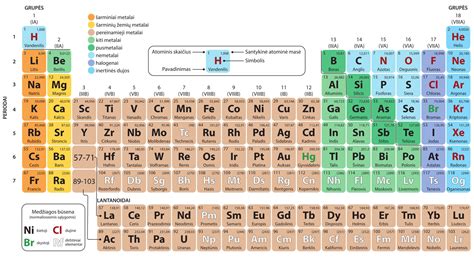
Halogenai - periodinės elementų sistemos VII A grupės cheminiai elementai, tokie kaip fluoras, chloras, bromas, jodas ir astatas. Pavadinimas „halogenas“ (iš graikų kalbos „gimdantis druską“) pirmą kartą buvo pasiūlytas chlorui 1811 m., o vėliau pritaikytas visiems triados nemetalams.
Jodo atradimas yra susijęs su Napoleono karų laikotarpiu, kai Prancūzijoje reikėjo suintensyvinti kalio salietros, svarbios parako sudedamosios dalies, gamybą. Savo ruožtu, tai paskatino didesnį potašo poreikį. Salietros gamintojas B. Kurtua (Prancūzija), ieškodamas potašo šaltinio, nusprendė panaudoti jūrų dumblius, kuriuos audros išmesdavo į krantą.
Kurtua pastebėjo, kad dumblių pelenų tirpale yra neįprastos medžiagos, kurią galima lengvai išskirti. Į tirpalą įpylus sieros rūgšties ir pakaitinus retortoje, sujungtoje su rinktuvu, nusėsdavo juodi milteliai, kurie kaitinami virsdavo violetiniais garais. Šie garai kondensavosi į blizgančias kristalines plokšteles, primenančias kristalinio švino sulfido blizgesį.
Po kelių dienų nuo Kurtua atradimo paskelbimo, Gei Liusakas Imperatoriškojo instituto posėdyje išsamiai aprašė naująją medžiagą. Jis įrodė, kad ši medžiaga analogiška chlorui, ir pasiūlė Kurtua preparatą pavadinti jodu (iš graikų kalbos „iodes“ - violetinis), atsižvelgiant į garų spalvą ir chloro pavadinimą.
Gamtoje halogenų laisvų nebūna, nes jie yra labai chemiškai aktyvūs. Jodas paplitęs jodatų pavidalu, o jodidų mineralų randama nedaug. Pavyzdžiui, natrio jodato (NaIO3) galima rasti kaip priemaišos Čilės salietroje (NaNO3). Kiti jodatų mineralai yra lautaritas Ca(IO3)2 ir dietzeitas 7Ca(IO3)2•8CaCrO4.
Jodo Paplitimas ir Gavimas
Jodo gamtoje esama beveik visur, tačiau labai mažomis koncentracijomis. Žinduolių organizme jodas kaupiasi kaip organiniai junginiai, dažniausiai tiroidinas skydliaukėje. Sutrikus skydliaukės funkcionavimui, gresia pavojus susirgti sunkiomis ligomis, tokiomis kaip Bazedovo liga ir kretinizmas.
Statistiniai duomenys rodo, kad tam tikruose Žemės rutulio plotuose (kalnuotose vietovėse) šios ligos yra paplitusios. Tai siejama su jodo trūkumu dirvožemyje ir biosferoje, nes šie rajonai nutolę nuo jūrų ir vandenynų, kurie yra pagrindiniai jodo koncentratai.
Bazedovo ligos profilaktikai pakanka įleisti tik 1 g jodo į 100 000 000 g komunalinio vandens. Sausumos augalai, kaip ir jūros dumbliai, gerai išskiria jodą iš dirvos ir koncentruoja savo organizme, jei dirvoje yra minimalus jo kiekis.
Lietuvoje nemažai jodo esama gręžinių vandenyje (nuo 10 iki 100 mg jodo litre), o Čilėje - Čilės salietros telkiniuose (0,2% masės).
Daugiausia jodo gaunama iš naftingų rajonų gręžinių vandens, kuriame jodo būna 30-100 mg/l. Iš čia jodas pirmiausia pradėtas gauti Lietuvoje, o vėliau šiuo šaltiniu pradėta naudotis Jungtinėse Amerikos Valstijose.
Jūrų vandenyje yra tik 0,05 mg/l jodo, tačiau laminariečiai sugeba jį sukoncentruoti iki 0,45% savo sausos masės. Japonijoje iš šių augalų 1960 m. buvo išgaunamas jodas. Iš tirpalo jodas išpučiamas karštais vandens garais arba oru, po to sukoncentruojamas (oksidacija, prapūtimas), o galutinai išvalomas resublimacija. Taikomas ir toks metodas: chloru oksiduotas vanduo veikiamas jonitais, jodas absorbuojamas polijodido pavidalu ir iš jo išgaunamas šarmais, o jonitai regeneruojami NaCl.
24 Faktai Apie : Jūrų dumbliai / Supermaistas
Jodo Panaudojimas
Jodas reikalingas farmacijos pramonei. Alkoholiniu jodo tirpalu dezinfekuojamos žaizdos. Neorganiniai junginiai plačiai naudojami chemijos laboratorijose. Apie 50% pagaminamo jodo suvartojama jo organinių junginių gamyboje, apie 15% - resublimuoto I2, KI ir kitų neorganinių junginių gamyboje.
Jodo reikia sintetinio kaučiuko ir katalizatorių gamyboje, jis vartojamas kaip stabilizatorius, dažanti medžiaga, rašalo pigmentas ir farmacinė medžiaga. Analizinėje chemijoje, pasinaudojant KHI3, gaminamas Neslerio reagentas K2[HgI4] (amoniakui aptikti).
Kambario temperatūroje jodas yra violetiniai metališko blizgesio kristalai, turintys molekulinę gardelę, todėl yra lakus. Kaitinamas sublimuojasi - virsta violetiniais garais. Vėsdami jodo garai neskystėdami kristalinasi. Jodas vandenyje tirpsta blogai, geriau - organiniuose tirpikliuose (benzole, anglies disulfide, alkoholyje, eteryje). Krakmolą jodas nudažo mėlynai, o jodido jonai I¯ krakmolo nenudažo. Kalio jodidas vartojamas medicinoje.
Halogenų Reaktingumas
Halogenų reaktingumas mažėja eilėje: F2>Cl2>Br2>I2. Didėjant halogeno atomo numeriui, jo trauka elektronams ir jonizacijos potencialas mažėja, t. y. elementų eilės F-Cl-Br-I elektroneigiamumas sumažėja. Jodas stipriai traukia labiausiai elektroteigiamus metalus.
Aliuminio gabalėlis, įmestas į skystą bromą, savaime lydosi nuo reakcijos šilumos ir juda bromo paviršiuje tarsi įkaitęs iki baltumo lašas, kol baigiasi jungimosi reakcija. Tuo pagrindu Tarybų Sąjungoje sukurtas metodas išskirti jodą iš naftos vandens.
Svarbiausi Jodo Junginiai
Svarbiausias jodo junginys yra vandenilio jodidas HI. HI kambario temperatūroje yra bespalvės dviaatomės dujos (tvir. 35,1°C). Jis gerai tirpsta vandenyje, susidaro vandenilio jodido rūgštis, stipriausia iš visų vandenilio halogenidų. HI sintetinamas iš elementų 300°C temperatūroje (katalizatorius Pt). Bevandenis HI yra energingas agentas metalams, nemetalams, hidridams, oksidams ir daugeliui kitų junginių klasių, dauguma šių reakcijų vyksta tik vartojant katalizatorius, šildant arba šviesoje.
Daugelis prieš pereinamuosius metalus esančių metalų (IA, IIA ir IIIA) grupių oksidaciniuose laipsniuose 2+ ir 3+ sudaro halogenidus, kuriuose dominuoja joninis charakteris.
Būdinga HI savybė yra sudaryti aceotropinius mišinius. Pašildžius praskiestą vandenį jų tirpalą iki virimo, HI koncentracija garuose būna mažesnė nei tirpale. Verdant tirpalo koncentracija palaipsniui didėja; virimo temperatūrai padidėjus iki tam tikros reikšmės, tirpalo sudėtis pasidaro tokia pati kaip ir dujų fazės. Toks mišinys vadinamas aceotropiniu.
Aceotropinio HI-H2O mišinio sudėtis, % HI, ir virimo temperatūra, °C, 1 atm. slėgyje yra tokia: 56,7 ir 126,7. Aceotropinio mišinio sudėtis rodo, iki kiek galima sukoncentruoti garinamus HI tirpalus.
Halogenai egzotermiškai jungiasi tarpusavyje, sudarydami stecheometrijų XY1, XY3, XY5, XY7 interhalogenidus, kur X - sunkesnis halogenas. Žinomi visi galimi dviaatomiai junginiai tarp F, Cl, Br, I. Šių junginių savybės yra tarpinės tarp juos sudarančių halogenų savybių. Tetraatominiai interhalogenidai yra ClF3, BrF3, IF3.
I2O5, I4O9, I2O4 - tai patvariausi oksidai. I2O5 gaunamas jodo rūgšties dehidratacija 200°C temperatūroje sauso oro srovėje arba tiesiogine jodo oksidacija deguonimi. I2O5 sudaro baltus higroskopinius termodinamiškai patvarius kristalus, labai tirpius vandenyje, kurie jame sudaro HIO3 (jodo rūgštį).
Žinomos mažiausiai keturios perjodatų - ortoperjodato (paraperjodato) rūgšties H5IO6 deprotonizacijos, dehidratacijos ir agregacijos serijos. Veikiant koncentruotai HNO3 iš bario paraperjodato gaunami perjodato rūgšties tirpalai, o iš jų - balti H5JO6 kristalai.
Protonizuojant ortoperjodato rūgštį koncentruotomis HClO4 arba H2SO4, susidaro katijonas [I(OH)6]+, užbaigiantis V periodo elementų heksahidrokso dalelių seriją: [Sn(OH)6]2¯, [Sb(OH)6]¯, [Te(OH)6], [I(OH)6]+.
Jodo Biologinė Svarba
Jodas yra skydliaukės hormono tiroksino sudedamoji dalis. Jis aktyvina medžiagų apykaitą, skatina oksidacijos reakcijas, tonizuoja raumenis. Trūkstant jodo, susergama struma. Šia liga dažniau serga kalnų rajonų gyventojai, kur vandenyje labai mažai jodo. Žmogui per parą reikia apie 3mg I/1 kg kūno masės.
Į sotų 20-25°C temperatūros kalio jodido tirpalą maišant pridedama jodo (iki prisotinimo). Mišinys atšaldomas iki 0°C temperatūros. Iškritusieji tamsiai rudi prizminiai KJ3•H2O kristalai nusiurbiami pro stiklinį filtrą, džiovinami tarp filtravimo popieriaus lapų ir sudedami į pritrintu kamščiu butelį ar užlydomi ampulėje. KJ3 yra higroskopiškas.
| Elementas | Savybės | Panaudojimas |
|---|---|---|
| Jodas (I) | Violetiniai kristalai, sublimuojasi | Dezinfekcija, farmacijos pramonė, analizinė chemija |
| Chloras (Cl) | Dujos | Dezinfekcija, chemijos pramonė |
| Bromas (Br) | Skystis | Chemijos pramonė, farmacijos pramonė |
| Fluoras (F) | Dujos | Branduolinė energetika, chemijos pramonė |